Basiskennis chemie/Bindingen/Ionbinding
Uiterlijk
Ionbinding
In tegenstelling tot de twee andere bindingstypen worden bij de ionbinding geen elektronen gedeeld, maar volledig overgedragen van het ene atoom op het andere. Een atoom waarvan het totaal aantal elektronen niet overeenkomt met de lading in de kern wordt een ion genoemd.
Het resultaat is wel dat er een positief en een negatief deeltje zijn ontstaan, die elkaar aantrekken. In een stukje lithiumfluoride zullen de groepjes van 2 ionen, een lithium-ion en een fluor-ion,[1] zo naast elkaar gaan liggen dat de positieve kant van het ene groepje tegen de negatieve kant van het andere zal komen. Op die manier ontstaat een lange rij afwisselend positief en negatief geladen deeltjes die stevig aan elkaar gebonden zijn door de elektrische aantrekkingskracht.
Er zijn twee soorten ionen:
- Negatieve ionen. Zij hebben meer elektronen dan overeenkomt met hun kernlading, een overschot aan elektronen. Omdat ze worden aangetrokken door de positieve elektrode, de anode,[2] worden die ionen anion genoemd.
- Positieve ionen. Zij hebben een tekort aan elektronen dus ook een tekort aan negatieve lading om de lading in de kern te neutraliseren. Zij zijn positief geladen. Dergelijke ionen worden door de negatieve kathode aangetrokken en heten daarom: kationen.
Elektriciteit
Een nieuw groepje van een lithium-ion en een fluor-ion[1] hoeft niet aan het einde van de rij aan te sluiten. Ergens halverwege ernaast kan ook. Wel is dan de voorwaarde dat het positieve lithium-ion naast een negatief geladen fluor-ion komt en het fluor-ion naast een positief geladen lithium-ion. Ook voor de richtingen omhoog en omlaag geldt dat.
LiF
Wat hierboven gezegd is voor de verbinding tussen lithium en fluor geldt voor alle verbindingen tussen elementen aan de linkerzijde en het midden van het periodiek systeem met elementen aan de rechterkant ervan. De elementen aan de linkerkant en in het midden staan allemaal makkelijk elektronen af, de elementen aan de rechterkant nemen de elektronen makkelijk op.
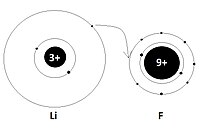
Het buitenste elektron van lithium gaat van een afstand van 152 pm[3], waar effectief maar een kernlading van 1+ actief is, naar een afstand van 133 pm in het fluoride-ion waar een effectieve kernlading van 7+ heerst. De kernlading die de elektronen in de valentieschil "zien" is voor beide ionen 2 lager doordat de elektronen in de eerste schil met hun lading een deel van de kernlading afschermen.

Het buitenste elektron van lithium gaat van een afstand van 152 pm[3], waar effectief maar een kernlading van 1+ actief is, naar een afstand van 133 pm in het fluoride-ion waar een effectieve kernlading van 7+ heerst. De kernlading die de elektronen in de valentieschil "zien" is voor beide ionen 2 lager doordat de elektronen in de eerste schil met hun lading een deel van de kernlading afschermen.
Vorming LiF
Zouten
Stoffen waarin de binding tussen de deeltjes ontstaan door het compleet overdragen van elektronen worden zouten genoemd. Het bekendste zout is uiteraard keukenzout, maar ook stoffen als soda, gips en roest worden in de chemie tot de zouten gerekend. Bij allemaal wordt de binding tussen de deeltjes in stand gehouden door elektrische krachten. Deze zijn ontstaan doordat sommige atomen elektronen hebben afgestaan en andere elektronen hebben opgenomen.
In de figuur hiernaast is met gekleurde knikkers aangegeven hoe je je dat voor moet stellen.
De manier waarop de deeltjes in een zoutkristal aan elkaar gebonden zijn heeft gevolgen voor de eigenschappen van zouten.Zouten zijn slechte elektrische geleiders
Er zijn in een zout geen elektronen aanwezig die makkelijk van het ene atoom naar het andere kunnen bewegen. Een zout is daarom een slechte geleider. Beter kun je zouten elektrische isolatoren noemen.
Dat verandert als het zout smelt. In een vloeibaar zout kunnen de geladen deeltjes wel langs elkaar bewegen. Als de polen van een batterij in het gesmolten zout gestoken worden bewegen de ionen naar de pool waar ze door aangetrokken worden.
Zouten zijn slechte warmtegeleiders
Ook voor warmte zijn zouten slechte geleiders. Om in een zoutkristal deeltjes sneller te laten trillen moet eigenlijk het hele kristal wat groter worden om ruimte te maken voor die beweging. Alleen meer ruimte op de plek waar de warmte wordt toegevoerd betekent dat de rangschikking van de positieve en negatieve ladingen ergens verstoord moet worden!
Warmte
Zouten zijn bros
Als materiaal bros genoemd wordt wil dat zeggen dat het hard is en dus moeilijk van vorm verandert. Het wil ook zeggen dat áls er vormverandering optreedt, dat ook meten 'breken' betekent. Met de positief en negatief geladen deeltjes kun je dat goed verklaren:
Op het moment dat twee lagen ionen langs elkaar schuiven is het eerste effect dat de positieve ionen niet meer netjes naast een negatief ion liggen, maar naast een positief geladen deeltje. Elektrisch positief en elektrisch positief stoot elkaar af. Een kleine verschuiving heeft meteen een volledige breuk van het kristal tot gevolg.
In de figuren hiernaast is dat weergegeven.Samengestelde ionen
Bij het bespreken van de covalente binding is alleen het delen van elektronen tussen atomen ter sprake gekomen. Soms heeft het delen van elektronen tot gevolg dat sommige elektronen er "een beetje bij hangen", soms ontstaat de situatie dat er ruimte is voor nog een of enkele extra elektronen. In die gevallen ontstaan samengestelde ionen. "Hangt het elektron er bij" dan wordt het makkelijk afgestaan en ontstaat een positief samengesteld ion, is er ruimte voor extra elektronen dan ontstaan samengestelde negatieve ionen.
In het hoofdstuk over de naamgeving van zouten staat een lijst van de belangrijkste samengestelde ionen, met hun naam, lading en chemische formule.
- ↑ 1,0 1,1 In de inhoud staat dit onderwerp voor de naamgeving. De uitgang ~ide blijft hier om didactische redenen daarom nog even onder de pet.
- ↑ In een introductie van de chemie hoeft de definitie die in de elektrochemie gemaakt wordt nog niet te worden aangebracht. Bovendien zijn de begrippen oxidatie en reductie hier nog niet aan de orde geweest.
- ↑ BINAS, 5e druk, Tabel 40A.






